老年痴呆(专业版)
老年痴呆,又称阿尔茨海默病,是一种破坏脑细胞的疾病,一种以认知功能下降为特征的神经变性疾病,并能最终导致死亡。患有这种疾病的人逐渐失去学习、思维和记忆等能力。这是最常见的
英文名称:Alzheimer's Dementia,Alzheimer's Disease
定义
老年痴呆,又称阿尔茨海默病,是一种破坏脑细胞的疾病,一种以认知功能下降为特征的神经变性疾病,并能最终导致死亡。患有这种疾病的人逐渐失去学习、思维和记忆等能力。这是最常见的痴呆症。老年痴呆症分为3个阶段:
- 早期阶段:失去记忆、推理、理解或学习能力,但不影响独立性。
- 中间阶段:脑损失增加,人格改变,并增加了对他人的基本需求依赖。
- 晚期阶段:身体功能和人格基本散失,完全依赖别人照顾。
病因
阿尔茨海默病的病因尚不完全清楚。- 在本病发展起主要作用的因素:
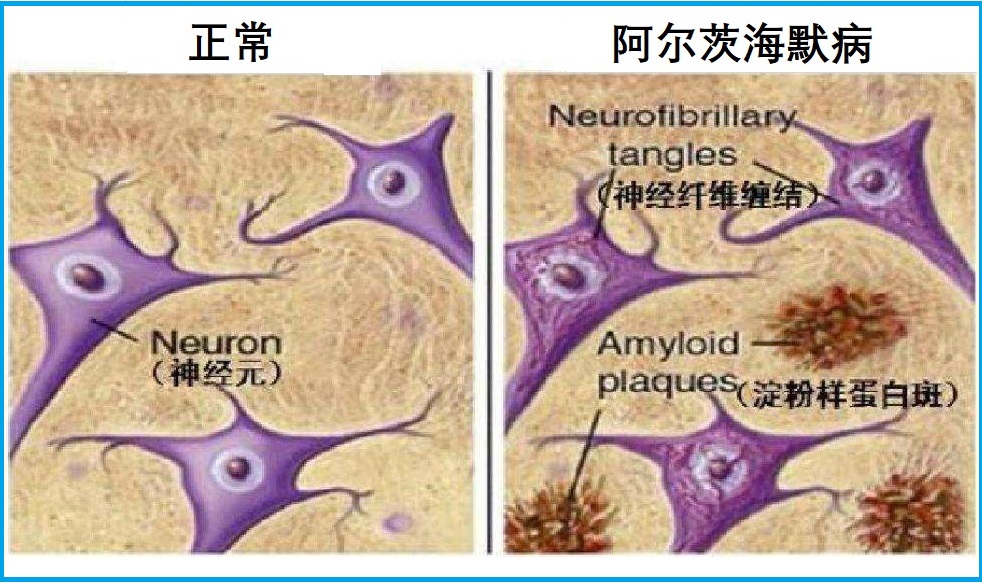
- β淀粉样蛋白(老年斑):在大脑的不同区域异常沉积的物质。这些斑块破坏脑细胞、干扰信号传输,并导致细胞死亡等。
- 神经原纤维缠结:在神经细胞内扭曲的纤维(称为Tau纤维蛋白,负责营养和其他必需物输送),引起脑细胞功能障碍,并最终导致脑细胞衰亡。
- 其他可能参与发病的因素可能包括如下:
- 缺乏乙酰胆碱,它是最主要的神经递质。
- 氧化应激。
- 慢性低度炎症。
- 脑细胞线粒体功能障碍,老化的原因和结果。
- 兴奋性毒性,谷氨酸是脑中最丰富的兴奋性神经递质,过多则对神经元有毒性作用,如促进老年斑形成、神经原纤维缠结、细胞器障碍和氧化应激等。
- 性激素水平下降,大脑性激素受体密度大,激素不足可显著影响到脑功能。
- 感染。
风险因素
65岁以上的人患老年痴呆的风险明显增加。65岁之前发病的,被称为早老性痴呆。其他可能增加患痴呆症的因素包括如下:
- 阿尔茨海默病家族史,尤其直系亲属。
- 存在某种类型蛋白(APOE-e4)。
- 唐氏综合征,可比常人提前10-20年发病。
- 女性比男性患病比率高,不过可能与女性寿命更长有关。
- 轻度认知功能障碍。
- 以前发生过严重的、创伤性脑损伤
- 一些不良生活方式,如:
- 缺乏运动锻炼、活动
- 肥胖
- 吸烟,或曝露于二手烟
- 高血压
- 高胆固醇
- 高同型半胱氨酸血症
- 脑卒中
- 动脉粥样硬化
- 控制不良的糖尿病
- 饮食缺乏蔬菜、水果
- 受教育程度低
- 缺乏社交关系、交流
- 营养不足或失衡
- 抑郁症
- 儿童期营养不良,维生素缺乏。·
- 血液中存在过多金属,尤其是锌、铜、铝、铁。
- 某些病毒感染。
症状
这种病起始于轻微的健忘或轻度思维混乱,随着时间推移,逐渐丧失更多和更深的记忆和脑功能,但症状恶化的速度因人而异。常见症状包括如下:
- 记忆问题表现为如:
- 反复陈述和提问题,而不是意识到它们之前已经问过
- 忘记对话、约会或发生的事件,以后再不记住它们
- 常常错置物品,经常把它们放在不合理的地方
- 如何做简单的数学计算。
- 无法找到正确的词语来识别对象,表达想法或参与对话
- 在熟悉的地方迷路
- 最终忘记家庭成员名字、日常物品和公共场所名称等
- 对日期、时间、季节遗忘。
- 思考和推理如:
- 老年痴呆症难以专注和思考,尤其是关于数字等抽象概念。
- 多任务处理特别困难,管理财务、日常开支账目等,可能会导致无法识别和处理数字。
- 做出判断和决定如:有效应对日常问题变得越来越困难,如炉灶上的食物燃烧或意外驾驶情况等。
- 个性和行为的变化,包括:
- 冷漠、面无表情
- 抑郁症
- 社交退缩,或躲避社交
- 情绪波动
- 对别人不信任
- 易怒和攻击性
- 改变睡眠习惯
- 流浪、行走缓慢
- 失去控制
- 妄想症,如相信某些东西被盗
并发症
随着老年痴呆发展到末期阶段,大脑变化开始影响身体功能,如吞咽、平衡和肠和膀胱控制,因而导致其他健康问题如:- 将食物或液体吸入肺部
- 肺炎和其他感染
- 跌倒、骨折
- 褥疮
- 营养不良或脱水
疗法
阿尔茨海默病还没有办法治愈。有些药物可以治疗一些症状、延缓病程发展。综合选项包括如下:
调整饮食与生活方式
- 健康饮食,富含优质蛋白、深海鱼和坚果,及新鲜蔬菜、水果
- 适度饮酒,不可过量
- 不抽烟,或戒烟
- 定期运动锻炼,尤其是各种有氧运动
- 保持脑力活跃,如参加社交活动、智力游戏等。
营养与草本综合干预
以下是基于循证医学和营养学有关文献综合的结果。
有助于防控阿尔茨海默病的营养和草本主要包括如下:
第一部分:与阿尔茨海默症相关的营养研究
1. 硫辛酸:
在动物研究中,这种强效抗氧化剂已被证明可以减少炎症、螯合金属和增加乙酰胆碱水平1,2。尽管只有少数几项关于硫辛酸与阿尔茨海默氏症的小型人体研究,但研究结果仍有希望。在一项研究中,9名阿尔茨海默氏症或类似痴呆症患者每天服用600mg硫辛酸,平均服用337天。在研究开始时,认知得分持续下降。到研究结束时,它们已经稳定下来3。第二项研究将这一方案扩展到43名患者,持续48个月,疾病进展极其缓慢(与未经治疗的患者的典型疾病进展率相比)4。
2. 乙酰L肉碱:
乙酰L肉碱(ALC)是一种抗氧化剂,已被证明可以纠正体内的乙酰胆碱缺陷,并通过支持健康的线粒体来保护神经元免受淀粉样蛋白β的影响5-7。一组研究人员将ALC与硫辛酸结合,发现它们可以逆转衰老动物的一些线粒体衰变。同一研究小组对ALC治疗轻度认知障碍和轻度阿尔茨海默病的21项临床试验进行了全面审查。他们发现ALC组与安慰剂组相比有显著的益处8。
ALC已被注意到可降低小鼠高同型半胱氨酸水平的影响(例如,血脑屏障完整性恶化、淀粉样蛋白β水平升高、神经原纤维缠结形成和认知功能障碍)9。此外,一项针对阿尔茨海默病患者的小型临床试验表明,在一年的时间里,每天3000mg ALC可显著减少认知能力的恶化10。实验室研究发现,ALC可以通过影响淀粉样蛋白前体蛋白代谢来降低淀粉样蛋白β的神经毒性11。
3. 维生素C和维生素E:
维生素C和E以其抗氧化特性而闻名。几项研究已经检验了它们在减少与阿尔茨海默病相关的氧化损伤方面的综合潜力12,13。一项观察性研究表明,补充维生素C(500mg/天)和维生素E(400IU/天)与降低阿尔茨海默病患病率有关14。另一组研究人员发现,维生素C和E的组合与降低阿尔茨海默病的风险有关,但这两种补充剂都不能单独提供实质性的保护15。然而,一项安慰剂对照临床试验发现,每天高达2000IU的高剂量维生素E可以减缓阿尔茨海默病患者的精神恶化,在动物模型中,维生素C有助于减少淀粉样蛋白β聚集16。
阿尔茨海默氏症患者维生素E缺乏与脂质过氧化增加有关,脂质过氧化似乎会增加血小板聚集17。维生素C和E的联合治疗已被证明可以减少轻度至中度阿尔茨海默病患者的脂质过氧化18。维生素C和E的高摄入量可能与健康老年人阿尔茨海默氏症的发病率降低有关19。
维生素E保护阿尔茨海默病的一种方法与它与载脂蛋白E4(apoE4)的关系有关。研究人员怀疑,在apoE4表型的人中,神经元抗氧化防御系统受损可能会增加氧化损伤20。另一种理论认为,维生素E可能能够减少大量诱导型一氧化氮合酶引起的氧化损伤,一氧化氮合酶是一种与阿尔茨海默病进展有关的促氧化剂21。此外,最近的一项研究表明,维生素E可以对抗淀粉样蛋白β诱导的氧化应激,这是阿尔茨海默病的一个特征22。(注意:诱导型一氧化氮合酶不应与维持健康动脉功能所需的内皮型一氧化氮合酶类混淆。)
3. 银杏叶:
银杏叶是一种抗氧化剂,可以作为抗炎剂,减少血液凝固,调节神经传递23,24。在一项研究中,银杏在轻度至中度阿尔茨海默病痴呆患者身上进行了测试。结果不一致。然而,在一个有神经精神症状的患者亚组中,与安慰剂相比,在26周内每天服用120–240mg银杏显著改善了认知能力25。另一项研究发现,银杏抑制大脑中淀粉样蛋白β的产生26。
银杏,如果与其他支持大脑的营养物质有效结合,似乎可以提供协同认知效果,部分原因是它能够改善脑血管功能27。研究表明,将银杏与磷脂酰丝氨酸、B族维生素和维生素E等其他营养素相结合,可以为动物和人类带来认知益处28。此外,一项研究发现,银杏提取物可以通过一种不同于其抗氧化特性的机制,从β淀粉样蛋白诱导的细胞死亡中拯救神经元细胞29。银杏似乎还可以通过抑制淀粉样纤维的形成来预防阿尔茨海默病30。最后,一项对六项研究的综述发现,银杏有益于认知和精神病理学症状,没有负面副作用的证据31。
4. 姜黄素:
许多研究表明,姜黄素可能是阿尔茨海默症的有效治疗方法,因为它通过多种途径发挥神经保护作用,包括抑制淀粉样蛋白β、清除现有的淀粉样蛋白α、抗炎作用、抗氧化活性、延迟神经元降解以及铜和铁的螯合等32-35。
姜黄素被发现可以减少认知功能障碍、神经突触损伤、淀粉样斑块沉积和氧化损伤。还发现它可以调节大脑神经元中细胞因子的水平33,36。姜黄素的抗炎作用似乎是由核因子κB(NF-κB)的减少引起的,NF-κB是一种调节许多参与细胞因子产生的基因的核转录因子37。姜黄素螯合铁和铜等有毒金属并降低其水平的能力也可能有助于防止淀粉样蛋白聚集38。姜黄素通过抑制与重金属(如镉和铅)的相互作用,可以减少大脑的失调33。实验室研究还表明,姜黄素在抑制动物大脑中淀粉样蛋白β积累方面比非处方非甾体抗炎药布洛芬和萘普生更有效39。一项临床试验发现,在27名可能患有阿尔茨海默病的受试者中,每天1至4g的常规姜黄素剂量耐受性良好,具有抗炎作用,并可能减少淀粉样蛋白β聚集40。
5. 石杉碱甲:
它是一种NMDA受体阻滞剂,可帮助预防或减少谷氨酸介导的兴奋性毒性41。它还可以帮助阻断乙酰胆碱酯酶,这是一种破坏乙酰胆碱的酶,对认知和记忆至关重要。这种作用机制类似于几种阿尔茨海默病药物,如多奈哌齐和加兰他敏42。一些研究表明,石杉碱甲可以穿透血脑屏障,具有更高的生物利用度,并且比一些药物具有更长的作用时间43,44。尽管并非所有关于石杉碱甲的研究都显示出对认知的积极影响45,但对先前研究的回顾显示,每天300-500mcg的石杉碱A剂量显著提高了阿尔茨海默病患者的标准化认知测试分数,并且比一些药物替代品略为安全46。
6. 猴头菇(狮鬃菇):
猴头菇是一种药食同源的蘑菇,在亚洲传统上用于提高记忆力47-49。在这种蘑菇中发现的一些主要有益成分包括β-葡聚糖多糖,猴头菇素(Erinacine)A、C、S和倍半萜49,50。几项实验室和动物研究报告称,猴头菇的化合物具有降脂、抗氧化、抗高血压、神经保护、抗肿瘤、抗菌和免疫刺激作用47,49,51。
在一项双盲安慰剂对照临床试验中,被诊断为轻度认知障碍的50至80岁的日本男性和女性接受了250mg含有96%蘑菇干粉的猴头菇片,每天三次,持续16周。八周后,猴头菇组的认知得分高于安慰剂组,并且在补充期间持续改善52。
在阿尔茨海默病小鼠模型中,口服30天的猴头菇提取物减少了动物大脑中淀粉样蛋白的产生和沉积,并支持脑细胞的生长。在同一项研究中,为期五个月的长期给药有助于恢复认知能力下降53。猴头菇提取物对认知的益处得到了对阿尔茨海默病小鼠模型的其他研究的支持,这些研究发现,该提取物改善了神经细胞的形成,减少了细胞损伤,并恢复了动物的一些行为缺陷50。在另一项针对阿尔茨海默病小鼠的研究中,猴头菇提取物提高了血清和大脑中神经递质乙酰胆碱的水平,而在阿尔茨海默病中,乙酰胆碱的水平会下降54-56。在神经元损伤的大鼠中,猴头菇的水提取物促进了外周神经的再生57。
在另一种小鼠模型中,补充猴头菇提取物阻断了炎症信号传导,并逆转了压力引起的抑郁样行为58。考虑到高达50%的阿尔茨海默病患者经历过抑郁症,这些发现意义重大59-61。在健康小鼠中也观察到了益处,其中口服补充猴头菇提取物可以改善与认知功能和情绪有关的大脑区域的识别记忆和神经传递62。
实验室研究表明,从猴头菇中分离的提取物或化合物支持神经元生长和存活47。在实验室实验中,猴头菇水提取物具有神经保护作用,并减少了细胞内活性氧的积累54。
7.苯磷硫胺:
苯磷硫胺是一种脂溶性维生素B1(硫胺素),作用于多种代谢途径,包括限制晚期糖基化终产物(AGEs)的产生。AGEs是葡萄糖与蛋白质非酶促相互作用形成的代谢产物,对身体有害。苯磷硫胺还显示出抗炎和抗氧化活性。在一些临床前模型中,苯磷硫胺已证明对GSK-3的抑制作用,GSK-3是一种与包括阿尔茨海默病在内的多种疾病的发病机制有关的酶63,64。在阿尔茨海默病的动物模型中,给予苯磷硫胺已显示出前景:给予苯磷硫胺的动物已被证明具有降低淀粉样蛋白β和磷酸化tau蛋白水平、恢复神经发生和改善记忆的作用65。
在一项为期12个月的双盲、随机、安慰剂对照试验中,70名患有轻度认知障碍或轻度阿尔茨海默症痴呆症的参与者接受了苯磷硫胺或安慰剂治疗。试验结束时,与安慰剂组相比,服用苯磷硫胺的参与者认知能力下降较少。具体而言,与安慰剂组相比,苯磷硫胺组的阿尔茨海默病评估量表认知亚量表(ADAS-Cog)得分和临床痴呆评分分别减少了43%和77%。此外,与安慰剂相比,苯磷硫胺降低了血清AGEs水平。在没有ApoE4变异基因的参与者中,苯磷硫胺的作用似乎更强65。在一项针对5名轻度至中度阿尔茨海默病患者的小型临床研究中,参与者在18个月内每天接受300mg苯磷硫胺治疗,到试验结束时,他们的迷你精神状态检查(MMSE)评分平均提高了3.2分66。
8. 亚洲参:
人参皂苷是人参提取物中的固醇类化合物,被认为是产生记忆益处的活性化学物质67。一项在没有认知问题的健康患者身上测试了200、400和600mg人参的研究发现,400mg人参在给药后1-6小时内产生了最大的益处并增强了记忆力68。当对58名阿尔茨海默病患者进行更高剂量的测试时,与同期认知能力下降的39名对照患者相比,在12周内每天服用4.5g人参可产生逐渐增加的改善,尽管这种改善在停药12周后消退69。
第二部分:与认知衰减和痴呆症相关的营养干预
1. DHA:一种主要存在于深海鱼类的ω-3脂肪酸,与认知功能有关70。DHA占人脑总脂肪酸含量的30%至50%71。它已被证明可以减少淀粉样蛋白β的分泌72并增加磷脂酰丝氨酸水平73。研究表明,ω-3脂肪酸有能力抑制神经原纤维缠结形成的早期阶段74,并减少淀粉样斑块的形成75。在一项涉及485名与年龄相关的认知能力下降患者的随机研究中,六个月内每天900mg DHA可显著改善学习和记忆测试76。
DHA发挥作用的一种方式是与其他保护性化合物协同作用,如类胡萝卜素77。在一项双盲、安慰剂对照、随机临床试验中78,轻度-中度AD患者在12个月内每天食用1g鱼油(其中500mg DHA、150mg EPA)、22mg类胡萝卜素(10mg叶黄素、10mg玉米黄质、2mg玉米黄素)和15mg维生素E或安慰剂。使用迷你精神状态检查(MMSE)和痴呆严重程度评定量表工具测量AD严重程度,行为、情绪和记忆使用基于信息者的问卷进行测量。
补充12个月后,与安慰剂组(n=27)相比,活性组(n=50)在皮肤类胡萝卜素测量、血液类胡萝卜素、ω-3FAs和维生素E浓度方面表现出统计学上的显著改善(p均<0.05)。活动组在AD严重程度的客观测量(即记忆力和情绪)方面也表现更好,据报道,记忆力的临床辅助指标存在统计学上的显著差异(p<0.001)。作者总结道“…鉴于该试验显示的积极结果,在AD的总体管理中应考虑这种联合微量营养素膳食补充剂。”78
2. 长春西汀:
主要来源于长春花植物,具有神经保护特性并增加大脑循环79,80。它还可以防止兴奋性毒性81。长春西汀在东欧已被用作治疗年龄相关记忆障碍的药物82。在一项对照临床试验中,每天三次10mg长春西汀改善了血管性老年性脑功能障碍受试者的各种认知功能指标83。注意:怀孕或计划怀孕的妇女不应使用长春西汀。
3. 丝氨酸磷脂(PS):
PS是一种天然存在的细胞膜成分。在日本对78名轻度认知障碍的老年人进行的一项研究中,补充PS六个月可显著改善记忆功能84。在另一项研究中,18名与年龄相关的记忆力下降的老年受试者在12周内每天3次服用100mg PS。6周和12周的测试显示,与基线测量相比,认知能力有所提高85。一组研究人员研究了含有丝氨酸磷脂的ω-3脂肪酸(PS-omega-3)对8名有记忆障碍的老年患者的安全性和有效性86,他们发现PS-omega-3对记忆功能有良好的影响。研究人员现在发现,补充丝氨酸磷脂与DHA的效果最佳87。
4. 吡咯喹啉醌(PQQ):
PQQ是一种重要的营养素,可刺激衰老细胞中新线粒体的生长,并促进线粒体的保护和修复88,89。线粒体衰退导致许多与年龄相关的疾病,包括阿尔茨海默氏症90,91。实验室研究表明,PQQ可能抑制阿尔茨海默病的发展92,93。PQQ保护神经元免受淀粉样蛋白β和蛋白α-突触核蛋白的影响,这有助于帕金森病的神经退行性变92,94。
每天补充20mg PQQ可改善一组中老年人的高级认知功能测试95。当受试者每天也服用300mg辅酶Q10时,这些效果显著增强。
5. 甘磷酰胆碱(GPC):
GPC是脑细胞膜的结构成分,也是神经递质乙酰胆碱的前体。在阿尔茨海默病中,由于神经退行性过程中细胞膜的破坏,CSF(脑脊液)中GPC的浓度增加96。补充GPC和其他营养物质,如乙酰L肉碱、DHA、α-硫辛酸和丝氨酸磷脂,可改善小鼠的认知功能97。一项针对261名阿尔茨海默型痴呆患者的临床试验显示,使用乙酰胆碱前体可以改善认知症状98。一项更大规模的试验还显示,当中风康复的患者服用1000-1200mg α-GPC 5个月时,认知能力显著改善99。
6. 类胡萝卜素:
类胡萝卜素是一种红-黄-橙色的植物色素,有助于防止植物关键成分受到光损伤。类胡萝卜素根据其化学结构可分为两类:叶黄素类(Xanthophylls,如虾青素、叶黄素、玉米黄质)和胡萝卜素(如β-胡萝卜素)。许多类胡萝卜素存在于健康、丰富多彩的食物中,如水果和蔬菜。一些类胡萝卜素已被证明可以轻易地穿过血脑屏障,并在中枢神经系统中发挥神经保护作用,包括抗氧化和抗凋亡作用100。其他证据表明,类胡萝卜素可能直接与β淀粉样蛋白结合,抑制大脑中有毒蛋白质的聚集101。
- 虾青素:虾青素在一些微藻中高度浓缩,并为许多甲壳类动物和鱼类提供颜色。与其他类胡萝卜素一样,虾青素具有强烈的抗炎和清除自由基的特性102,103。由于虾青素已被证明可以穿过血脑屏障,人们对其保护脑组织免受年龄变化影响的能力越来越感兴趣。最近的证据表明,虾青素促进大脑可塑性,从而有可能预防或改善与年龄相关的认知障碍102,104。许多临床前研究表明,虾青素通过多种机制有助于保持神经和记忆健康105-107。
- 叶黄素和玉米黄质:叶黄素和玉米黄质在人类视网膜和黄斑中含量很高。因此,叶黄素和玉米黄质通常被称为“黄斑色素”或“黄斑类胡萝卜素”114。考虑到眼睛和中枢神经系统之间的密切解剖联系115,黄斑和血液中的叶黄素和玉米黄质水平与认知显著相关也就不足为奇了。事实上,这些黄斑类胡萝卜素似乎可以预防认知障碍的发展116,117。
第三部分:支持认知功能的营养
1. 镁(苏糖酸镁):
镁参与NMDA型谷氨酸受体的功能,这是记忆处理的组成部分。研究发现,血清镁水平失衡会导致认知障碍125,126。最近研究发现,一种名为L-苏氨酸镁(MgT)的专利配方镁化合物(苏糖酸镁Magtein®)比其他形式的镁更有效地提高大脑中的镁水平。这些较高的脑镁水平改善了突触信号传导,这对正常的神经元和认知功能以及增强长期学习和记忆至关重要。对动物进行的MgT测试显示,记忆力,尤其是长期记忆力有了显著改善127。
苏糖酸镁(1500-2000mg)似乎可以缓解老年人的认知能力下降128。一项随机、双盲、安慰剂对照研究检查了Magtein(MMFS-01)对老年人认知能力下降的影响。共有44名患有轻度认知障碍的参与者(年龄50-70岁)每天服用安慰剂或MMFS-01(25mg/kg体重),持续12周。与安慰剂相比,MMFS-01组经历了认知能力和认知波动的改善,随着时间的推移心智能力的大幅波动(例如“糟糕的日子”)。他们的认知功能几乎恢复到健康成年人的水平。研究者称:“目前的研究证明了MMFS-01在治疗老年人认知障碍方面的潜力。”
2. 维生素B族:
高同型半胱氨酸水平以及低水平的B族维生素(如叶酸、维生素B12和维生素B6)与阿尔茨海默病和轻度认知障碍有关129,130。
- 叶酸:已知DNA合成需要叶酸。在一项包括30名阿尔茨海默病患者的研究中,晚发性阿尔茨海默病患者脑脊液中叶酸水平显著降低131。另一项针对70至79岁人群的纵向分析发现,高血同或叶酸水平低的人认知功能受损。叶酸水平低与认知障碍的联系最强,研究人员认为补充叶酸可能会降低认知能力下降的风险132。
- 维生素B12:在一项评估阿尔茨海默病或另一种痴呆症患者维生素B12水平的研究中,研究人员发现,B12水平较低与认知能力恶化有关133。一项针对75岁或75岁以上无痴呆症人群的纵向研究发现,在三年内,维生素B12或叶酸水平低的人群患阿尔茨海默病的风险是其他人群的两倍134。
- 维生素B6:一项研究发现,与对照受试者相比,60岁后的阿尔茨海默病患者摄入的维生素B6量明显较低135。此外,维生素B6水平低与阿尔茨海默病患者大脑病变数量增加有关136。
- 维生素B3(烟酸):1993年至2002年间,一项针对6000多人的研究发现,高水平的膳食烟酸(维生素B3)可以预防阿尔茨海默病。作者研究了65岁及以上健康人群的饮食习惯。随着研究的进展,一些参与者患上了阿尔茨海默病,一些人保持健康。烟酸摄入量最高的受试者认知能力下降的风险降低了70%137。
3. 维生素D:
维生素D受体在大脑中的广泛分布可能是维生素D在神经功能中重要性的证据138。研究表明,足够水平的维生素D可以促进淀粉样蛋白β通过血脑屏障的清除。动物试验表明,补充维生素D可以使淀粉样蛋白的清除率提高1.3倍,这表明它对阿尔茨海默病具有潜在的预防作用139。在近500名随访7年的女性中,维生素D摄入量最高的五分之一女性患阿尔茨海默病的风险比摄入量最低的五分之一女性降低了75%以上140。
4. 辅酶Q10:
CoQ10可改善涉及线粒体功能丧失的几种神经退行性疾病的预后141,142。研究表明,阿尔茨海默病患者的辅酶Q10水平会发生变化143,补充辅酶Q10是改善阿尔茨海默病患者线粒体功能的综合方法的一部分144。
在一项动物研究中,辅酶Q10抵消了接受β淀粉样蛋白治疗的大鼠的线粒体缺陷145,而在另一项实验中,辅酶Q10减少了β淀粉样蛋白质的过量产生146。在实验室研究中,辅酶Q10也显示出破坏淀粉样蛋白斑块的稳定性147。
一些临床试验评估了合成辅酶Q10类似物对阿尔茨海默病患者的影响,并显示出良好的结果。例如,一项在203名阿尔茨海默病患者中比较药物乙酰胆碱酯酶抑制剂他克林(Tacrine)和辅酶Q10类似物的试验表明,辅酶Q10相似物在一些标准化认知评估中有更大的改善148。另一项试验显示,与安慰剂相比,接受CoQ10类似物治疗的阿尔茨海默病患者的认知评估有剂量依赖性改善。该试验还表明CoQ10类似物是安全且耐受性良好的149。同样,在一项针对102名阿尔茨海默病患者的试验中,与安慰剂相比,辅酶Q10类似物改善了记忆力、注意力和行为150。
5. N-乙酰半胱氨酸:
N-乙酰半胱氨酸(NAC)是谷胱甘肽的前体,谷胱甘肽是体内自由基的强大清除剂151,152。谷胱甘肽缺乏与许多神经退行性疾病有关153。一项研究表明,NAC显著提高了用已知自由基产生剂治疗的啮齿类动物的谷胱甘肽水平并降低了氧化应激153。另一项研究表明,谷胱甘肽缺乏的小鼠更容易受到β淀粉样蛋白的神经元损伤154。阿尔茨海默症动物模型发现NAC减轻了氧化损伤和认知能力下降155。
6. 复合维矿素:
在阿尔茨海默病患者中观察到多种营养缺乏156,157。最近,科学家们发现,血清中维生素B、C、D和E的生物标志物水平较高,以及鱼类中最常见的ω-3油(EPA和DHA)水平较高的人,大脑萎缩或认知功能下降的可能性较小158。
一项针对14名早期阿尔茨海默氏症患者的人体研究发现,多种营养素的配方改善了所有认知指标,尽管记忆功能的改善在统计上并不显著。该制剂包括400mcg叶酸、6mcg维生素B12、30 IU维生素E、400mg S-腺苷蛋氨酸(SAM-E)、600 mg N-乙酰半胱氨酸和500 mg乙酰L肉碱。在为期12个月的研究中,认知能力持续改善159。在一项针对200名没有认知或记忆问题的健康中年人的研究中,与仅服用安慰剂的组相比,服用复合维生素2个月的人在认知功能测试中得分更高,在长期认知挑战中表现出更少的疲劳,获得了更高的准确性,并且在数学处理方面证明更快160。
7. 预防老年痴呆特医食品Souvenaid®:
欧盟认可的特殊医学营养食品,含有动植物蛋白及多种复合维生素等,用于改善前驱期及早期阿尔茨海默病(AD)相关的轻度认知障碍、维持记忆功能等161,162。
8. 咖啡和咖啡因:
对几项研究的回顾表明,饮用咖啡可以降低患阿尔茨海默氏症和帕金森症的风险163。小鼠长期服用咖啡因可以通过抑制β和γ分泌酶来减少大脑淀粉样蛋白β的沉积。一个动物模型显示,咖啡因似乎与另一种咖啡成分协同作用,提高血液中粒细胞集落刺激因子(G-CSF)的水平。更高的G-CSF水平和长期服用含咖啡因的咖啡都被证明可以增强工作记忆164。
绿原酸是一种存在于咖啡中的抗氧化多酚,已被证明可以降低血压、全身炎症、2型糖尿病风险和血小板聚集164,165。在一项研究中,当短期或工作记忆受损的小鼠服用绿原酸时,它们的认知障碍显著逆转166。多酚的可用性因咖啡豆的烘焙时间和烘焙方法本身而异。所有的烘焙都会破坏一些多酚,其中最重要的是绿原酸。绿原酸的一种来源是绿咖啡豆提取物167。
9. 绿茶:
绿茶中的多酚即儿茶素(EGCG),已被证明具有金属螯合(结合)特性,以及抗氧化和抗炎作用168。动物研究表明,EGCG以及其他茶儿茶素,可以降低大脑中淀粉样蛋白β的水平169,并抑制淀粉样蛋白诱导的认知功能障碍和神经毒性170,171。研究表明,EGCG还可以调节神经元信号和代谢、细胞存活和死亡基因以及线粒体功能。最近,基于人群的研究确定,绿茶和红茶中摄入儿茶素可以降低阿尔茨海默病和痴呆症的发病率172。
10. 葡萄籽(提取物):
葡萄籽提取物是含有原花青素的强效抗氧化剂173。在实验室研究中,动物神经元在暴露于β淀粉样蛋白之前用葡萄籽提取物处理。与未经处理的神经元容易积累自由基并随后死亡不同,用葡萄籽提取物处理的细胞受到了显著的保护174。在另一项动物研究中,服用葡萄籽多酚可以减少大脑中淀粉样蛋白β的聚集,减缓阿尔茨海默病样认知障碍175。
11. 白藜芦醇:
白藜芦醇已被证明可以降低淀粉样蛋白β水平、神经毒性、细胞死亡和海马体退化,并预防学习障碍176。几项研究表明,适量饮用红酒尤其与痴呆症和阿尔茨海默病的发病率较低有关177。研究表明,红酒中还含有许多酚类抗氧化化合物,这些化合物会阻碍阿尔茨海默病的病理进展178。还观察到,在阿尔茨海默氏症模型中,白藜芦醇的衍生物己烯类化合物可以降低淀粉样蛋白β肽的聚集179。白藜芦醇已被证明可以选择性地中和有害的淀粉样肽团块,同时保持良性肽的完整性180。
12. 南非醉茄:
一种在印度阿育吠陀医学用于治疗各种与年龄相关的疾病的著名植物181。2012年一项使用阿尔茨海默病动物模型的研究发现,南非醉茄逆转了淀粉样肽的积累,改善了行为缺陷182。实验室研究表明,南非醉茄可以再生轴突(即神经细胞的突起),并在严重受损的神经元中重建突触183。除了其神经保护作用外,南非醉茄还被证明可以模仿阿尔茨海默病药物多奈哌齐(一种乙酰胆碱酯酶抑制剂)的作用184。
13. 蓝莓:
2005年,科学家们注意到蓝莓中的多酚可以逆转衰老引起的认知和运动缺陷185。蓝莓提取物刺激神经发生并增强海马体的神经元可塑性(适应性),海马体是大脑中主要受阿尔茨海默病影响的区域186。在一项研究中,研究人员分析了水果和蔬菜的抗氧化能力,蓝莓位居榜首,其中和自由基的能力得分最高187。
14. 野燕麦:
来自野生绿燕麦的野燕麦提取物(Avena sativa L.)含有具有抗氧化和抗炎特性的生物活性成分188。它含有黄酮类化合物、皂苷和燕麦特有的化合物-燕麦生物碱(Avenanthramides)189, 190。
单胺氧化酶B(MAO-B)活性的增加降低了大脑中的多巴胺水平,并增加了神经元中的氧化应激191,192。对阿尔茨海默病死者脑组织的分析发现,其MAO-B活性是健康、年龄匹配的对照组脑组织的三倍193, 194。
单胺氧化酶抑制剂被认为是治疗阿尔茨海默病的有前途的治疗靶点,因为它们能够减少β淀粉样蛋白的积累并改善认知和记忆缺陷195,196。野生绿燕麦提取物能够抑制MAO-B活性189,197。
患有轻度认知障碍的老年患者在单次服用1600mg野燕麦提取物后,在认知测试中表现明显更好198。参加一项双盲安慰剂对照试验的健康中年人在单次服用800mg野生绿燕麦提取物后,在多项认知测试中的表现有所改善199。
15. 提高NAD+水平:
NAD+是NAD的一种生物活性形式,对Sirtuins的激活是必需的。Sirtuins是调节细胞代谢和DNA转录的蛋白质200-202。依赖NAD+的Sirtuins似乎参与能量代谢、DNA损伤反应、应激抵抗、增殖和分化、存活和衰老等基本细胞活动,在动物研究中已被证明可以调节大脑连接和记忆形成203,204。NAD+水平随着年龄的增长而降低,这可能会导致细胞核和线粒体功能障碍,最终导致一系列与年龄相关的疾病,包括认知能力下降和阿尔茨海默病204,202。在神经退行性过程的实验细胞模型中,NAD、NAD+和烟酰胺核糖防止了神经元和神经元连接的破坏205,206。补充烟酰胺核苷恢复NAD+已被证明可以逆转与年龄相关的细胞功能障碍,这会导致许多神经退行性疾病,而阿尔茨海默病的模型表明烟酰胺核苷可能具有神经保护作用202,207。
在一项对26名可能患有阿尔茨海默病的患者进行的为期六个月的对照试验中,与安慰剂组相比,接受NADH(烟酰胺腺嘌呤二核苷酸,又称脱氢酶)治疗的患者认知能力下降没有进展,在痴呆症评定量表上的得分明显更好208。在啮齿类动物中,老年动物服用NADH可提高认知测试的表现209。在阿尔茨海默病小鼠模型中,三个月的烟酰胺核糖核补充可提高大脑NAD+水平,防止认知能力下降,并降低神经元损伤性淀粉样蛋白β蛋白的水平210。除了烟酰胺核糖、脱氢酶NDAH外,NMN(β-烟酰胺单核苷酸)也可以提高NAD+水平。
更多可点击其个性化的综合干预方案如下:
- 痴呆症防控要略(抗毒性蛋白)
- 痴呆症防控要略(改善认知记忆)
- 痴呆症防控要略(维持神经递质)
- 痴呆症防控要略(降低氧化应激)
- 痴呆症防控要略(防线粒体障碍)
- 痴呆症防控要略(抑制发展)
- 早老性痴呆防控(65岁前)
- 老年痴呆防控(早期)
- 老年痴呆防控(中期)
- 老年痴呆防控(晚期)
以及参阅本网如下专文的相关内容:
医疗干预
常规治疗措施包括如下:
已被批准用于减少老年痴呆症的药物包括2种:
- 胆碱酯酶抑制剂,提高乙酰胆碱水平,治疗轻、中度阿尔茨海默病。
- 美金刚胺(NMDA),用于中至重度阿尔茨海默病。
此外,患有老年痴呆的人可能会出现精神症状,可能需要精神类药物治疗如:
- 抗抑郁药
- 抗焦虑药物
- 抗精神病药
注意:病患护理者支持,因为照顾老年痴呆症患者困难、很累人。因此,护理者需要情感支持、休息和定期休假。
家庭护理
老年痴呆生活方式管理,应包括如下内容:
- 创造一个可以得到的需要护理环境。
- 尽可能保持较高的生活质量。
- 保持自身的安全。
- 学会和妥善应对无法控制的行为挫折。
- 有个平静、安稳、可预测的环境。
- 提供合适的眼镜、助听器,易于阅读的时钟和日历。
- 听听轻柔的音乐。
- 做轻型和适当运动,减少躁动和缓解抑郁。
- 鼓励家庭和亲密的朋友经常光顾。
预防
因为发病确切的原因未知,没有预防阿尔茨海默症的指南。但以下措施有助于降低患老年痴呆的风险:- 健康饮食,包括深海鱼类。
- 适度饮酒,适量饮酒可以降低患痴呆症的风险。然而,饮酒过量可增加患痴呆症的风险。
- 经常运动锻炼。
- 参加能刺激脑力的活动,包括社交、智力游戏等。
- 控制好慢性病,如心脑血管疾病的中间风险因素(“三高”)等。
参考文献:
1. Bitar MS et al. Inflammation and apoptosis in aortic tissues of aged type II diabetes: amelioration with alpha-lipoic acid through phosphatidylinositol 3-kinase/Akt- dependent mechanism. Life Sci. 2010 Jun 5;86(23-24):844-53.
2. Holmquist L, et al. Lipoic Acid as a Novel Treatment for Alzheimer’s disease and Related Dementias. Pharmacol Thera. 113.1 (2007): 154-164.
3. Hager K et al. Alpha-Lipoic Acid as a New Treatment Option for Alzheimer [corrected] Type Dementia. Arch Gerontol Geriatr. 2001 Jun;32(3):275-82.
4. Hager K et al. Alpha-Lipoic Acid as a New Treatment Option for Alzheimer's Disease-A 48 Months Follow-up Analysis. J Neural Transm Suppl. 2007;(72):189-93.
5.Butterworth RF. Evidence for Forebrain Cholinergic Neuronal Loss in Congenital Ornithine Transcarbamylase Deficiency. Metab Brain Dis. 2000 Mar;15(1):83-91.
6. Dhitavat S et al. Folate, Vitamin E, and Acetyl-L-Carnitine Provide Synergistic Protection against Oxidative Stress Resulting from Exposure of Human Neuroblastoma Cells to Amyloid-Beta. Brain Res. 2005 Nov 9;1061(2):114-7.
7. Virmani MA et al. The Acti on of Acetyl-L-Carnitine on the Neurotoxicity Evoked by Amyloid Fragments and Peroxide on Primary Rat Cortical Neurones. Ann N Y Acad Sci. 2001 Jun;939:162-78.
8. Ames BN et al. Delaying the Mitochondrial Decay of Aging with Acetylcarnitine. Ann N Y Acad Sci. 2004 Nov;1033:108-16.
9. Zhou P et al. Acetyl-L-Carnitine Attenuates Homocysteine-Induced Alzheimer-Like Histopathological and Behavioral Abnormalities. Rejuvenation Res. 2011 Dec;14(6):669-79.
10. Pettegrew JW et al. Clinical and Neurochemical Effects of Acetyl-L-Carnitine in Alzheimer’s disease. Neurobiol Aging. 1995 Jan-Feb;16(1):1-4.
11. Epis R et al. Modulatory Effect of Acetyl-L-Carnitine on Amyloid Precursor Protein Metabolism in Hippocampal Neurons. Eur J Pharmocol. Nov 2008;597.1-3: 51-56.
12. Gehin A et al. Glyphosate-induced Antioxidant Imbalance in HaCaT: The Protective Effect of Vitamins C and E. Environ Toxicol Pharmocol. 2006 Jul;22(1):27-34.
13. Shireen KF et al. Effects of Dietary Vitamin E, C and Soybean Oil Supplementation on Antioxidant Enzyme Activities in Liver and Muscles of Rats. Food Chem Toxicol. Oct 2008;46.10: 3290-3294.
14. Boothby LA et al. Vitamin C and vitamin E for Alzheimer’s disease. Ann Pharmacother. 2005 Dec;39(12):2073-80.
15. Zandi PP et al. Reduced Risk of Alzheimer Disease in Users of Antioxidant Vitamin Supplements: The Cache County Study. Arch Neurol. 2004 Jan;61(1):82-8.
16. Cheng F et al. Suppression of Amyloid β A11 Antibody Immunoreactivity by Vitamin C: Possible Role Of Heparan Sulfate Oligosaccharides Derived From Glypican-1 By Ascorbate-induced, Nitric Oxide (NO)-catalyzed Degradation. J Biol Chem. 2011 Aug 5;286(31):27559-72.
17. Ciabattoni G et al. Determinants of Platelet Activation in Alzheimer’s Disease. Neurobiol Aging. 2007 Mar;28(3):336-42.
18. Galbusera C et al. Increased Susceptibility to Plasma Lipid Peroxidation in Alzheimer Disease Patients. Curr Alzheimer Res. 2004 May;1(2):103-9.
19. Landmark K. Could Intake of Vitamins C and E Inhibit Development of Alzheimer Dementia? [in Norwegian]. Tidsskr Nor Laegeforen. 2006 Jan 12;126(2):159-61.
20. Mas E et al. Functional Vitamin E Deficiency in ApoE4 Patients with Alzheimer’s Disease. Dement Geriatr Cogn Disord. 2006;21(3):198-204
21. McCann SM et al. The Nitric Oxide Theory of Aging Revisited. Ann N Y Acad Sci. 2005 Dec;1057:64-84.
22. Pocernich CB et al. Nutritional Approaches to Modulate Oxidative Stress in Alzheimer’s Disease. Curr Alzheimer Res. 2011 Aug;8(5):452-69.
23. Diamond BJ et al. Ginkgo biloba Extract: Mechanisms and Clinical Indications. Arch Phys Med Rehab. 2000 May;81(5):668-78.
24. Perry EK et al. Medicinal Plants and Alzheimer’s Disease: From Ethnobotany to Phytotherapy. J Pharm Pharmacol. 1999 May;51(5):527-34.
25. Schneider LS et al. A Randomized, Double-Blind, Placebo-Controlled Trial of Two Doses of Ginkgo biloba Extract in Dementia of the Alzheimer’s Type. Curr Alzheimer Res. 2005 Dec;2(5):541-51.
26. Yao ZX et al. Ginkgo biloba Extract (Egb 761) Inhibits Beta-Amyloid Production by Lowering Free Cholesterol Levels. J Nutr Biochem. 2004 Dec;15(12):749-56.
27. Mashayekh A et al. Effects of Ginkgo biloba on Cerebral Blood Flow Assessed by Quantitative MR Perfusion Imaging: A Pilot Study. Neuroradiology. 2011 Mar;53(3):185-91.
28. Araujo JA et al. Improvement of Short-Term Memory Performance in Aged Beagles by a Nutraceutical Supplement Containing Phosphatidylserine, Ginkgo biloba, Vitamin E, and Pyridoxine. Can Vet J. Can Vet J. 2008 Apr;49(4):379-85.
29. Aranda-Abreu GE et al. Rehabilitating a Brain with Alzheimer’s: A Proposal. Clin Interv Aging. 2011;6:53-9.
30. Longpré F et al. Protection by EGb 761 against Beta-Amyloid-Induced Neurotoxicity: Involvement of NF-KappaB, SIRT1, and Mapks Pathways and Inhibition of Amyloid Fibril Formation. Free Radic Biol Med. 2006 Dec 15;41(12):1781-94.
31. Janssen IM et al. Ginkgo biloba in Alzheimer’s Disease: A Systematic Review. Wien Med Wochenschr. 2010 Dec;160(21-22):539-46.
32. Begum AN et al. Curcumin Structure-Function, Bioavailability, and Efficacy in Models of Neuroinflammation and Alzheimer’s Disease. J Pharmacol Exp Ther. 2008 Jul;326(1):196-208.
33. Mishra S et al. The Effect of Curcumin (Turmeric) on Alzheimer’s Disease: An Overview. Ann Indian Acad Neurol. 11.1 (2008): 13-9.
34. Ringman JM et al. A Potential Role of the Curry Spice Curcumin in Alzheimer’s Disease. Curr Alzheimer Res. 2005 Apr;2(2):131-6.
35. Walker D et al. Anti-Inflammatory and Immune Therapy for Alzheimer’s Disease: Current Status and Future Directions. Curr Neuropharmacol. 2007 Dec;5(4):232-43.
36. Cole GM et al. NSAID and Antioxidant Prevention of Alzheimer’s Disease: Lessons from in Vitro and Animal Models. Ann N Y Acad Sci. 2004 Dec;1035:68-84.
37. Aggarwal BB et al. Suppression of the Nuclear Factor-KappaB Activation Pathway by Spice-Derived Phytochemicals: Reasoning for Seasoning. Ann N Y Acad Sci. 2004 Dec. 1030:434-441
38. Baum L et al. Curcumin Interaction with Copper and Iron Suggests One Possible Mechanism of Action in Alzheimer’s Disease Animal Models. J Alzheimers Dis. 2004 Aug;6(4):367-77
39. Yang F et al. Curcumin Inhibits Formation of Amyloid Beta Oligomers and Fibrils, Binds Plaques, and Reduces Amyloid in Vivo. J Biol Chem. 2005 Feb 18;280(7):5892-901.
40. Baum L et al. Six-Month Randomized, Placebo-Controlled, Double-Blind, Pilot Clinical Trial of Curcumin in Patients with Alzheimer Disease. [In eng] J Clin Psychopharmacol. 2008 Feb; 28(1): 110-3.
41. Wang XD et al. Modulation of NMDA receptor by huperzine A in rat cerebral cortex. Zhongguo Yao Li Xue Bao. 1999 Jan;20(1):31-5.
42. Sun QQ et al. Huperzine-A Capsules Enhance Memory and Learning Performance in 34 Pairs of Matched Adolescent Students. Zhongguo Yao Li Xue Bao. 1999 Jul;20(7):601-3.
43. Wang R et al. Progress in Studies of Huperzine A: A Natural Cholinesterase Inhibitor from Chinese Herbal Medicine. Acta Pharmacol Sin. 2006 Jan;27(1):1-26.
44. Bai DL et al. Huperzine A: A Potential Therapeutic Agent for Treatment of Alzheimer’s Disease. Curr Med Chem. 2000 Mar;7(3):355-74.
45. Rafii MS et al. A phase II trial of huperzine A in mild to moderate Alzheimer disease. Neurology. 2011 Apr;76(16):1389-94.
46. Wang BS et al. Efficacy and Safety of Natural Acetylcholinesterase Inhibitor Huperzine A in the Treatment of Alzheimer’s Disease: An Updated Meta-Analysis. J Neural Transm. 2009 Apr;116(4):457-65.
47. Zhang CC et al. Chemical Constituents from Hericium erinaceus Promote Neuronal Survival and Potentiate Neurite Outgrowth via the TrkA/Erk1/2 Pathway. International journal of molecular sciences. Jul 2017;18(8).
48. Phan CW et al. Hericium erinaceus (Bull.: Fr) Pers. cultivated under tropical conditions: isolation of hericenones and demonstration of NGF-mediated neurite outgrowth in PC12 cells via MEK/ERK and PI3K-Akt signaling pathways. Food Funct. Dec 2014;5(12):3160-3169.
49. Khan MA Tania M, Liu R, Rahman MM. Hericium erinaceus: an edible mushroom with medicinal values. Journal of complementary & integrative medicine. May 24 2013;10.
50. Tsai-Teng T et al. Erinacine A-enriched Hericium erinaceus mycelium ameliorates Alzheimer's disease-related pathologies in APPswe/PS1dE9 transgenic mice. J Biomed Sci. Jun 27 2016;23(1):49.
51. Zeng X et al. Proteome analysis provides insight into the regulation of bioactive metabolites in Hericium erinaceus. Gene. Aug 5 2018;666:108-115.
52. Mori K et al. Improving effects of the mushroom Yamabushitake (Hericium erinaceus) on mild cognitive impairment: a double-blind placebo-controlled clinical trial. Phytotherapy research. Mar 2009;23(3):367-372.
53. Tzeng TT et al. The Cyanthin Diterpenoid and Sesterterpene Constituents of Hericium erinaceus Mycelium Ameliorate Alzheimer's Disease-Related Pathologies in APP/PS1 Transgenic Mice. International journal of molecular sciences. Feb 2018;19(2).
54. Zhang J et al. The Neuroprotective Properties of Hericium erinaceus in Glutamate-Damaged Differentiated PC12 Cells and an Alzheimer's Disease Mouse Model. International journal of molecular sciences. Nov 1 2016;17(11).
55. Mufson EJ et al. Cholinergic system during the progression of Alzheimer's disease: therapeutic implications. Expert Rev Neurother. Nov 2008;8(11):1703-1718.
56. Kelley BJ et al. Alzheimer's disease and mild cognitive impairment. Neurologic clinics. Aug 2007;25(3):577-609.
57. Wong KH et al. Hericium erinaceus (Bull.: Fr.) Pers., a medicinal mushroom, activates peripheral nerve regeneration. Chin J Integr Med. Oct 2016;22(10):759-767.
58. Chiu CH et al. Erinacine A-Enriched Hericium erinaceus Mycelium Produces Antidepressant-Like Effects through Modulating BDNF/PI3K/Akt/GSK-3beta Signaling in Mice. International journal of molecular sciences. Jan 2018;19(2).
59. Lyketsos CG et al. Depression in Alzheimer's disease: overview and treatment. Biological psychiatry. Aug 1 2002;52(3):243-252.
60. Chi S et al. Depression in Alzheimer's disease: epidemiology, mechanisms, and management. Journal of Alzheimer's disease. 2014;42(3):739-755.
61. Modrego PJ. Depression in Alzheimer's disease. Pathophysiology, diagnosis, and treatment. Journal of Alzheimer's disease. 2010;21(4):1077-1087.
62. Brandalise F et al. Dietary Supplementation of Hericium erinaceus Increases Mossy Fiber-CA3 Hippocampal Neurotransmission and Recognition Memory in Wild-Type Mice. Evidence-based complementary and alternative medicine : eCAM. 2017;2017:3864340.
63. Sun XJ et al. Benfotiamine prevents increased β-amyloid production in HEK cells induced by high glucose. Neurosci Bull. 2012;28(5): 561-566.
64. Markova N et al. Thiamine and benfotiamine improve cognition and ameliorate GSK-3β-associated stress-induced behaviours in mice. Prog Neuropsychopharmacol Biol Psychiatry. 2017;75: 148-156.
65. Gibson GE et al. Benfotiamine and Cognitive Decline in Alzheimer's Disease: Results of a Randomized Placebo-Controlled Phase IIa Clinical Trial. J Alzheimers Dis. 2020;78(3): 989-1010.
66. Pan X et al. Long-Term Cognitive Improvement After Benfotiamine Administration in Patients with Alzheimer's Disease. Neurosci Bull. 2016;32(6): 591-596.
67. Christensen LP. Ginsenosides chemistry, biosynthesis, analysis, and potential health effects. Adv Food Nutr Res. 2009;55:1-99.
68. Kennedy DO et al. Dose Dependent Changes in Cognitive Performance and Mood Following Acute Administration of Ginseng to Healthy Young Volunteers. Nutr Neurosci. 2001;4(4):295-310.
69. Lee ST et al. Panax ginseng Enhances Cognitive Performance in Alzheimer Disease. Alzheimer Dis Assoc Disord. 2008 Jul-Sep;22(3):222-6.
70. Swanson D et al. Omega-3 fatty acids DHA and EPA: Health Benefits throughout Life. Adv Nutr. 2012 Jan;3(1):1-7.
71. Young G et al. Omega-3 Fatty Acids and Neuropsychiatric Disorders. Reprod Nutr Dev. 2005 Jan-Feb;45(1):1-28.
72. Lukiw WJ, et al. A Role for Docosahexaenoic Acid-Derived Neuroprotectin D1 in Neural Cell Survival and Alzheimer Disease. J Clin Invest. 2005 Oct;115(10):2774-83.
73. Akbar M, et al. Docosahexaenoic Acid: A Positive Modulator of Akt Signaling in Neuronal Survival. Proc Natl Acad Sci USA. 2005 Aug 2;102(31):10858-63.
74. Ma QL et al. Beta-Amyloid Oligomers Induce Phosphorylation of Tau and Inactivation of Insulin Receptor Substrate via C-Jun N-Terminal Kinase Signaling: Suppression by Omega-3 Fatty Acids and Curcumin. J Neurosci. 2009 Jul 15;29(28):9078-89.
75. Amtul Z et al. Structural Basis for the Differential Effects of Omega-3 and Omega-6 Fatty Acids on Abeta Production and Amyloid Plaques.” J Biol Chem. 2011 Feb 25;286(8):6100-7.
76. Yurko-Mauro K et al. Beneficial Effects of Docosahexaenoic Acid on Cognition in Age-Related Cognitive Decline. Alzheimers Dement. 2010 Nov;6(6):456-64.
77. Parletta N et al. Nutritional modulation of cognitive function and mental health. The Journal of nutritional biochemistry. May 2013;24(5):725-743.
78. Nolan JM et al. Supplementation with Carotenoids, Omega-3 Fatty Acids, and Vitamin E Has a Positive Effect on the Symptoms and Progression of Alzheimer's Disease. J Alzheimers Dis. 2022;90(1):233-249.
79. Szilagyi G et al. Effects of Vinpocetine on the Redistribution of Cerebral Blood Flow and Glucose Metabolism in Chronic Ischemic Stroke Patients: A PET Study. 2005 Mar 15;229-230:275-84.
80. Dézsi L et al. Neuroprotective Effects of Vinpocetine in Vivo and in Vitro: Apovincaminic Acid Derivatives as Potential Therapeutic Tools in Ischemic Stroken [in Hungarian]. Acta Pharm Hung. 2002;72(2):84-91.
81. Sitges M et al. Vinpocetine Blockade of Sodium Channels Inhibits the Rise in Sodium and Calcium Induced by 4-Aminopyridine in Synaptosomes. Neurochem Int. 2005; 46.7: 533-40.
82. Vinpocetine Monograph. Altern Med Rev. 2002;7(3): 240-3. Available at: http://www.altmedrev.com/publications/7/3/240.pdf Accessed 7/25/2012.
83. Balestreri R et al. A double-blind placebo controlled evaluation of the safety and efficacy of vinpocetine in the treatment of patients with chronic vascular senile cerebral dysfunction. J Am Geriatr Soc. 1987 May;35(5):425-30.
84. Kato-Kataoka A et al. Soybean-derived Phosphatidylserine Improves Memory Functions of the Elderly Japanese Subjects with Memory Complaints. J Clin Biochem Nutr. 2010 Nov;47(3):246-55.
85. Schreiber S et al. An Open Trial of Plant-Source Derived Phosphatydilserine for Treatment of Age-Related Cognitive Decline. Isr J Psychiatry Relat Sci. 2002; 37.4: 302-7.
86. Richter Y et al. The Effect of Phosphatidylserine-containing Omega-3 Fatty Acids on Memory Abilities in Subjects with Subjective Memory Complaints: A Pilot Study. Clin Interv Aging. 2010; 5: 313–316.
87. Shyh-Hwa L et al. Docosahexaenoic Acid and Phosphatidylserine Supplementations Improve Antioxidant Activities and Cognitive Functions of the Developing Brain on Pentylenetetrazol-Induced Seizure Model. Brain Res. 2012 Apr 27;1451:19-26.
88. Chowanadisai W et al. Pyrroloquinoline quinone stimulates mitochondrial biogenesis through cAMP response element-binding protein phosphorylation and increased PGC-1alpha expression. J Biol Chem. 2010; 285.1: 142-152.
89. Tao R et al. Pyrroloquinoline quinone preserves mitochondrial function and prevents oxidative injury in adult rat cardiac myocytes. Biochem Biophys Res Commun. 2007 Nov 16;363(2):257-62.
90. Facecchia K et al. Oxidative Toxicity in Neurodegenerative Diseases: Role of Mitochondrial Dysfunction and Therapeutic Strategies. J Toxicol. 2011;2011:683728.
91. Martin LJ. Mitochondrial and Cell Death Mechanisms in Neurodegenerative Diseases. Pharmaceuticals (Basel). 2010, 3(4), 839-915.
92. Kim J et al. The Inhibitory Effect of Pyrroloquinoline Quinone on the Amyloid Formation and Cytotoxicity of Truncated Alpha-Synuclein. Mol Neurodegener. 5 (2010): 20.
93. Liu S et al. Enhanced Rat Sciatic Nerve Regeneration through Silicon Tubes Filled with Pyrroloquinoline Quinone. Microsurgery. 25.4 (2005): 329-37.
94. Zhang JJ et al. Protective Effect of Pyrroloquinoline Quinone against Abeta-Induced Neurotoxicity in Human Neuroblastoma SH-SY5Y Cells. Neurosci Lett. 2009;464.3: 165-9.
95. Nakano M et al. Effect of pyrroloquinoline quinone (PQQ) on mental status of middle-aged and elderly persons. FOOD Style. 2009;21:13(7):50-3.
96. Walter A et al. Glycerophosphocholine is Elevated in Cerebrospinal Fluid of Alzheimer Patients. Neurobiol Aging. 2004;25.10: 1299-303.
97. Suchy J et al. Dietary supplementation with a combination of α-lipoic acid, acetyl-l-carnitine, glycerophosphocoline, docosahexaenoic acid, and phosphatidylserine reduces oxidative damage to murine brain and improves cognitive performance. Nut Res. 29.1 (2009): 70-74.
98. Moreno M. Cognitive improvement in mild to moderate Alzheimer’s dementia after treatment with the acetycholine precursor choline alfoscerate: A multicenter, double-blind, randomized, placebo-controlled trial. Clin Ther. 2003;25.1: 178-93.
99. Barbagallo Sangiorgi G et al. Alpha-Glycerophosphocholine in the mental recovery of cerebral ischemic attacks. An Italian multicenter clinical trial. Ann NY Acad Sci 1994; 717:253-69.
100. Park HA et al. Anti-Apoptotic Effects of Carotenoids in Neurodegeneration. Molecules (Basel, Switzerland). 2020 Jul;25(15):3453.
101. Lakey-Beitia J et al. Carotenoids as Novel Therapeutic Molecules Against Neurodegenerative Disorders: Chemistry and Molecular Docking Analysis. International journal of molecular sciences. 2019 Nov ;20(22):5553.
102. Grimmig B et al. Neuroprotective mechanisms of astaxanthin: a potential therapeutic role in preserving cognitive function in age and neurodegeneration. GeroScience. Feb 2017;39(1):19-32.
103. Guedes AC et al. Microalgae as sources of carotenoids. Marine drugs. 2011;9(4):625-644.
104. Wu H et al. Astaxanthin as a Potential Neuroprotective Agent for Neurological Diseases. Marine drugs. Sep 2015;13(9):5750-5766.
105. Sifi N et al. K(+) channel blocker-induced neuroinflammatory response and neurological disorders: immunomodulatory effects of astaxanthin. Inflammation research. Aug 2016;65(8):623-634.
106. Hongo N et al. Astaxanthin Ameliorated Parvalbumin-Positive Neuron Deficits and Alzheimer's Disease-Related Pathological Progression in the Hippocampus of App(NL-G-F/NL-G-F) Mice. Frontiers in pharmacology. 2020;11:307.
107. Taksima T et al. Effects of Astaxanthin from Shrimp Shell on Oxidative Stress and Behavior in Animal Model of Alzheimer's Disease. Mar Drugs. 2019;17(11):628.
108. Satoh A et al. Preliminary Clinical Evaluation of Toxicity and Efficacy of A New Astaxanthin-rich Haematococcus pluvialis Extract. Journal of clinical biochemistry and nutrition. May 2009;44(3):280-284.
109. Katagiri M et al. Effects of astaxanthin-rich Haematococcus pluvialis extract on cognitive function: a randomised, double-blind, placebo-controlled study. Journal of clinical biochemistry and nutrition. Sep 2012;51(2):102-107.
110. Nakagawa K et al. Antioxidant effect of astaxanthin on phospholipid peroxidation in human erythrocytes. The British journal of nutrition. Jun 2011;105(11):1563-1571.
111. Ito N et al. Effects of Composite Supplement Containing Astaxanthin and Sesamin on Cognitive Functions in People with Mild Cognitive Impairment: A Randomized, Double-Blind, Placebo-Controlled Trial. J Alzheimers Dis. 2018;62(4):1767-1775.
112. Yang X et al. Combining antioxidant astaxantin and cholinesterase inhibitor huperzine A boosts neuroprotection. Molecular medicine reports. 2020;21(3):1043-1050.
113. Alghazwi M et al. In vitro studies of the neuroprotective activities of astaxanthin and fucoxanthin against amyloid beta (Abeta1-42) toxicity and aggregation. Neurochemistry international. 2019;124:215-224.
114. Lima VC et al. Macular pigment in retinal health and disease. Int J Retina Vitreous. 2016 Aug 15;2:19.
115. Grzybowski A et al. OCT and Imaging in Central Nervous System Diseases: The Eye as a Window to the Brain. Springer Nature; Book. 2020.
116. Min JY et al. Serum lycopene, lutein and zeaxanthin, and the risk of Alzheimer's disease mortality in older adults. Dement Geriatr Cogn Disord. 2014;37(3-4):246-256.
117. Kelly D et al. Cognitive Function and Its Relationship with Macular Pigment Optical Density and Serum Concentrations of its Constituent Carotenoids. J Alzheimers Dis. 2015;48(1):261-277.
118. Mullan K, Williams MA, Cardwell CR, et al. Serum concentrations of vitamin E and carotenoids are altered in Alzheimer's disease: A case-control study. Alzheimer's & dementia (New York, N Y). 2017;3(3):432-439.
119. Renzi LM et al. Relationships between macular pigment optical density and cognitive function in unimpaired and mildly cognitively impaired older adults. Neurobiol Aging. 2014;35(7):1695-1699.
120. Feart C et al. Plasma Carotenoids Are Inversely Associated With Dementia Risk in an Elderly French Cohort. The journals of gerontology Series A, Biological sciences and medical sciences. 2016;71(5):683-688.
121. Nolan JM et al. Nutritional Intervention to Prevent Alzheimer's Disease: Potential Benefits of Xanthophyll Carotenoids and Omega-3 Fatty Acids Combined. J Alzheimers Dis. 2018;64(2):367-378.
122. Nolan JM et al. The impact of supplemental macular carotenoids in Alzheimer's disease: a randomized clinical trial. J Alzheimers Dis. 2015;44(4):1157-1169.
123. Power R et al. Supplemental Retinal Carotenoids Enhance Memory in Healthy Individuals with Low Levels of Macular Pigment in A Randomized, Double-Blind, Placebo-Controlled Clinical Trial. J Alzheimers Dis. 2018;61(3):947-961.
124. Singhrang N et al. Protective effects of silk lutein extract from Bombyx mori cocoons on beta-Amyloid peptide-inducedapoptosis in PC12 cells. Biomedicine & pharmacotherapy. 2018;103:582-587.
125. Corsonello A et al. Serum Magnesium Levels and Cognitive Impairment in Hospitalized Hypertensive Patients. Magnes Res. 2001;14.4: 273-82.
126. Barbagallo M et al. Altered ionised Magnesium Levels in Mild-to-Moderate Alzheimer’s Disease. Magnes Res. 2011 Sep;24(3):S115-21.
127. Slutsky I et al. Enhancement of Learning and Memory by Elevating Brain Magnesium. Neuron. 2010;65.2: 165-77.
128. Liu G et al. Efficacy and Safety of MMFS-01, a Synapse Density Enhancer, for Treating Cognitive Impairment in Older Adults: A Randomized, Double-Blind, Placebo-Controlled Trial. J Alzheimers Dis. 2016;49(4):971-90.
129. Quadri P et al. Homocysteine and B Vitamins in Mild Cognitive Impairment and Dementia. Clin Chem Lab Med. 2005;43.10:1096-100.
130. Ravaglia G et al. Homocysteine and Folate as Risk Factors for Dementia and Alzheimer Disease. Am J Clin Nutr. 2005;82.3: 636-43.
131. Serot JM et al. CSF-Folate Levels Are Decreased in Late-Onset AD Patients. J Neural Transm. 2001;108.1: 93-9.
132. Kado DM et al. Homocysteine versus the Vitamins Folate, B6, and B12 as Predictors of Cognitive Function and Decline in Older High-Functioning Adults: MacArthur Studies of Successful Aging. Am J Med. 118.2 (2005): 161-7.
133. Engelborghs S et al. Correlations between Cognitive, Behavioural and Psychological Findings and Levels of Vitamin B12 and Folate in Patients with Dementia. Int J Geriatr Psychiatry. 2004;19.4: 365-70.
134. Wang HX et al. Vitamin B(12) and Folate in Relation to the Development of Alzheimer’s Disease. Neurology. 2001;56.9: 1188-94.
135. Mizrahi EH et al. Plasma Total Homocysteine Levels, Dietary Vitamin B6 and Folate Intake in AD and Healthy Aging. J Nutr Health Aging. 2003;7(3):160-5.
136. Mulder C et al. Low Vitamin B6 Levels Are Associated with White Matter Lesions in Alzheimer’s Disease. J Am Geriatr Soc. 2005;53.6: 1073-4.
137. Morris MC et al. Dietary Niacin and the Risk of Incident Alzheimer’s Disease and of Cognitive Decline. J Neurol Neurosurg Psychiatry. 2004;75.8: 1093-9.
138. Eyles DW et al. Distribution of the Vitamin D Receptor and 1α-hydroxylase in Human Brain.” J Chem Neuroanat. 2005;29.1: 21-30.
139. Ito S et al. 1-alpha,25-Dihydroxyvitamin D3 Enhances Cerebral Clearance of Human Amyloid-Β Peptide(1-40) from Mouse Brain across the Blood-Brain Barrier. Fluids Barriers CNS. 2011 July; 8:20.
140. Annweiler C et al. Higher Vitamin D Dietary Intake Is Associated with Lower Risk of Alzheimer's Disease: A 7-Year Follow-Up. [In Eng] J Gerontol A Biol Sci Med Sci. 2012 Nov;67(11):1205-11.
141. Galpern WR et al. Coenzyme Q Treatment of Neurodegenerative Diseases of Aging. Mitochondrion. 2007 Jun;7 Suppl:S146-53.
142. Manacuso M et al. Coenzyme Q10 in Neuromuscular and Neurodegenerative Disorders. Curr Drug Targets. 2010;11.1: 111-21.
143. Dhanasekaran M et al. The Emerging Role of Coenzyme Q-10 in Aging, Neurodegeneration, Cardiovascular Disease, Cancer and Diabetes Mellitus. Curr Neurovasc Res. 2005;2.5: 447-59.
144. Kidd PM. Neurodegeneration from Mitochondrial Insufficiency: Nutrients, Stem Cells, Growth Factors, and Prospects for Brain Rebuilding Using Integrative Management. Altern Med Rev. 2005;10.4: 268-93.
145. Moreira PI et al. CoQ10 Therapy Attenuates Amyloid Beta-Peptide Toxicity in Brain Mitochondria Isolated from Aged Diabetic Rats.” Exp Neurol. 2005;196.1:112-9.
146. Yang X et al. Coenzyme Q10 Attenuates Beta-Amyloid Pathology in the Aged Transgenic Mice with Alzheimer Presenilin 1 Mutation. J Mol Neurosci. 2008;34.2:165-71.
147. Ono K et al. Preformed Beta-Amyloid Fibrils Are Destabilized by Coenzyme Q10 in Vitro. Biochem Biophys Res Commun. 2005;330.1: 111-6.
148. Gutzmann H et al. Safety and Efficacy of Idebenone Versus Tacrine in Patients with Alzheimer's Disease: Results of a Randomized, Double-Blind, Parallel-Group Multicenter Study. [In eng] Pharmacopsychiatry. 2002 Jan; 35(1): 12-8.
149. Gutzmann H et al. Sustained Efficacy and Safety of Idebenone in the Treatment of Alzheimer's Disease: Update on a 2-Year Double-Blind Multicentre Study. [In eng] J Neural Transm Suppl. 1998 54:301-10.
150. Senin U et al. Idebenone in Senile Dementia of Alzheimer Type: A Multicentre Study. [In eng] Arch Gerontol Geriatr. 1992 Nov-Dec; 15(3): 249-60.
151. Forman HJ et al. Glutathione: Overview of its Protective Roles, Measurement, and Biosynthesis. Mol Aspects Med. 30.1-2 (2009): 1-12.
152. Arakawa M et al. N-acetylcysteine and Neurodegenerative Diseases: Basic and Clinical Pharmacology. Cerebellum. 2007;6(4):308-14.
153. Pocernich CB et al. In Vivo Glutathione Elevation Protects against Hydroxyl Free Radical-Induced Protein Oxidation in Rat Brain. Neurochem Int. 36.3 (2000): 185-91.
154. Crack PJ et al. Lack of Glutathione Peroxidase-1 Exacerbates Abeta-Mediated Neurotoxicity in Cortical Neurons. J Neural Transm (Vienna). 2006 May;113(5):645-57.
155. Tchantchou F et al. N-Acetyl Cysteine Alleviates Oxidative Damage to Central Nervous System of Apoe-Deficient Mice Following Folate and Vitamin E-Deficiency. J Alzheimers Dis. 2005;7.2:135-8.
156. Kristensen MO, Gulmann NC, Christensen JE, et al. Serum cobalamin and methylmalonic acid in Alzheimer dementia. Acta Neurol Scand. 1993 Jun;87(6):475-81.
157. Jiménez-Jiménez FJ et al. Cerebrospinal Fluid Levels of Alpha-Tocopherol (Vitamin E) in Alzheimer’s Disease. J Neural Transm. 1997;104.6-7:703-10.
158. Bowman GL et al. Nutrient Biomarker Patterns, Cognitive Function, and MRI Measures of Brain Aging. Neurology. 2012 Jan 24;78(4):241-9.
159. Chan A et al. Efficacy of a Vitamin/Nutriceutical Formulation for Early-Stage Alzheimer’s Disease: A 1-Year, Open-Label Pilot Study with a 16-Month Caregiver Extension. Am J Alzheimers Dis Other Demen. 2008;23.6:571-85.
160. Haskell CF et al. Effects of a Multi-Vitamin/Mineral Supplement on Cognitive Function and Fatigue During Extended Multi-Tasking. Hum Psychopharmacol. 2010;25.6:448-61.
161. Scheltens P et al. Efficacy of Souvenaid in mild Alzheimer's disease: results from a randomized, controlled trial J Alzheimers Dis. 2012;31(1):225-36.
162. Soininen H, et al. 24-month intervention with a specific multinutrient in people with prodromal Alzheimer's disease (LipiDiDiet): a randomised, double-blind, controlled trial. Lancet Neurology. 2017;16(12):965-975.
163. Butt MS et al. Coffee and Its Consumption: Benefits and Risks. Crit Rev Food Sci Nutr. 2011;51.4:363-73.
164. Cao C et al. Caffeine Synergizes with Another Coffee Component to Increase Plasma GCSF: Linkage to Cognitive Benefits in Alzheimer’s Mice. J Alzheimers Dis. 2011;25.2 2011:323-35.
165. Montagnana M et al. Coffee Intake and Cardiovascular Disease: Virtue Does Not Take Center Stage. Semin Thromb Hemost. 2012 Mar;38(2):164-77.
166. Kwon SH et al. Neuroprotective Effects of Chlorogenic Acid on Scopolamine-Induced Amnesia via Anti-Acetylcholinesterase and Anti-Oxidative Activities in Mice. Eur J Pharmacol. 2010;649.1-3:210-7.
167. Jaiswal R et al. Profile and characterization of the chlorogenic acids in green Robusta coffee beans by LC-MS(n): identification of seven new classes of compounds. J Agric Food Chem. 2010;58.15:8722-37.
168. Mandel S et al. Green Tea Catechins as Brain-Permeable, Natural Iron Chelators-Antioxidants for the Treatment of Neurodegenerative Disorders. Mol Nutr Food Res. 2006;50.2: 229-34.
169. Rezai-Zadeh K et al. Green Tea Epigallocatechin-3-Gallate (EGCG) Modulates Amyloid Precursor Protein Cleavage and Reduces Cerebral Amyloidosis in Alzheimer Transgenic Mice. J Neurosci. 2005;25.38:8807-14.
170. Haque AM et al. Green Tea Catechins Prevent Cognitive Deficits Caused by Abeta1-40 in Rats. J Nutr Biochem. 2008;19.9:619-26.
171. Rezai-Zadeh K et al. Green Tea Epigallocatechin-3-Gallate (EGCG) Reduces Beta-Amyloid Mediated Cognitive Impairment and Modulates Tau Pathology in Alzheimer Transgenic Mice. Brain Res. 2008;12.1214:177-87.
172. Mandel SA et al. Understanding the Broad-Spectrum Neuroprotective Action Profile of Green Tea Polyphenols in Aging and Neurodegenerative Diseases. J Alzheimers Dis. 2011;25.2:187-208.
173. Shi J et al. Polyphenolics in Grape Seeds: Biochemistry and Functionality. J Med Food. 2003;6.4:291-9.
174. Li MH et al. Protective Effects of Oligomers of Grape Seed Polyphenols against Beta-Amyloid-Induced Oxidative Cell Death. Ann NY Acad Sci. 2004;1030:317-29.
175. Wang J et al. Grape-Derived Polyphenolics Prevent Alpha Beta Oligomerization and Attenuate Cognitive Deterioration in a Mouse Model of Alzheimer’s Disease. J Neurosci. 2008;28.25: 6388-92.
176. Kim D et al. SIRT1 Deacetylase Protects against Neurodegeneration in Models for Alzheimer’s Disease and Amyotrophic Lateral Sclerosis.” EMBO J. 2007;26.13:3169-79.
177. Vingtdeux V et al. Therapeutic potential of resveratrol in Alzheimer’s disease. BMC Neurosci. BMC Neurosci. 2008 Dec 3;9 Suppl 2(Suppl 2):S6.
178. Ho L et al. Heterogeneity in Red Wine Polyphenolic Contents Differentially Influences Alzheimer’s Disease-Type Neuropathology and Cognitive Deterioration. J Alzheimers Dis. 2009;16.1:59-72.
179. Richard T et al. Neuroprotective Properties of Resveratrol and Derivatives. Ann N Y Acad Sci. 2011;1215:103-8.
180. Ladiwala ARA et al. Resveratrol Selectively Remodels Soluble Oligomers and Fibrils of Amyloid Beta into Off-Pathway Conformers. J Biol Chem. 285 (2010): 24228-37.
181. Ven Murthy MR et al. Scientific Basis for the Use of Indian Ayurvedic Medicinal Plants in the Treatment of Neurodegenerative Disorders: Ashwagandha. Cent Nerv Syst Agents Med Chem. 2010;10.3:238-46.
182. Sehgal N et al. Withania somnifera reverses Alzheimer's disease pathology by enhancing low-density lipoprotein receptor-related protein in liver. Proc Natl Acad Sci U S A. 2012 Feb;109(9):3510-5.
183. Kuboyama T et al. Neuritic Regeneration and Synaptic Reconstruction Induced by Withanolide A.” Br J Pharmacol. 144.7 (2005): 961-71.
184. Choudhary MI et al. Cholinesterase Inhibiting Withanolides from Withania somnifera. Chem Pharm Bull Tokyo. 2004;52.11:1358-61.
185. Lau FC et al. The Beneficial Effects of Fruit Polyphenols on Brain Aging. Neurobiol Aging. 2005;26.1:128-32.
186. Casadesus G et al. Modulation of hippocampal plasticity and cognitive behavior by short-term blueberry supplementation in aged rats. Nutr Neurosci. 2004 Oct-Dec;7(5-6):309-16.
187. Wu X et al. Lipophilic and Hydrophilic Antioxidant Capacities of Common Foods in the United States. J Agric Food Chem. 2004;52.12: 4026-37.
188. Lee YM et al. Bioactives in Commonly Consumed Cereal Grains: Implications for Oxidative Stress and Inflammation. Journal of medicinal food.Nov 2015;18(11):1179-1186.
189. Wong RH et al. Chronic effects of a wild green oat extract supplementation on cognitive performance in older adults: a randomised, double-blind, placebo-controlled, crossover trial. Nutrients. May 2012;4(5):331-342.
190. Dimpfel W et al. Ingested oat herb extract (Avena sativa) changes EEG spectral frequencies in healthy subjects. Journal of alternative and complementary medicine. May 2011;17(5):427-434.
191. Nagatsu T, Sawada M. Molecular mechanism of the relation of monoamine oxidase B and its inhibitors to Parkinson's disease: possible implications of glial cells. Journal of neural transmission. Supplementum. 2006(71):53-65.
192. Mallajosyula JK et al. Metabolic control analysis in a cellular model of elevated MAO-B: relevance to Parkinson's disease. Neurotoxicity research.Oct 2009;16(3):186-193.
193. Saura J et al. Increased monoamine oxidase B activity in plaque-associated astrocytes of Alzheimer brains revealed by quantitative enzyme radioautography. Neuroscience. Sep 1994;62(1):15-30.
194. Jossan SS et al. Monoamine oxidase B in brains from patients with Alzheimer's disease: a biochemical and autoradiographical study. Neuroscience.1991;45(1):1-12.
195. Cai Z. Monoamine oxidase inhibitors: promising therapeutic agents for Alzheimer's disease (Review). Molecular medicine reports. May 2014;9(5):1533-1541.
196. Delumeau JC et al. Monoamine oxidase inhibitors, cognitive functions and neurodegenerative diseases. Journal of neural transmission. Supplementum.1994;41:259-266.
197. Moccetti T et al. Bioactivity-based development of a wild green oat (Avena sativa L.) extract in support of mental health disorders. Zeitschrift für Phytotherapie.2006;27(S1):P24.
198. Berry NM et al. Acute effects of an Avena sativa herb extract on responses to the Stroop Color-Word test. Journal of alternative and complementary medicine. Jul 2011;17(7):635-637.
199. Kennedy DO et al. Acute effects of a wild green-oat (Avena sativa) extract on cognitive function in middle-aged adults: A double-blind, placebo-controlled, within-subjects trial. Nutr Neurosci. 2017 Feb;20(2):135-151.
200. Houtkooper RH et al. The secret life of NAD+: an old metabolite controlling new metabolic signaling pathways. Endocr Rev. Apr 2010;31(2):194-223.
201. Chi Y et al. Nicotinamide riboside, a trace nutrient in foods, is a vitamin B3 with effects on energy metabolism and neuroprotection. Current opinion in clinical nutrition and metabolic care. Nov 2013;16(6):657-661.
202. Imai S et al. NAD+ and sirtuins in aging and disease. Trends Cell Biol. Aug 2014;24(8):464-471.
203. Gao J et al. A novel pathway regulates memory and plasticity via SIRT1 and miR-134. Nature. Aug 26 2010;466(7310):1105-1109.
204. Srivastava S. Emerging therapeutic roles for NAD(+) metabolism in mitochondrial and age-related disorders. Clinical and translational medicine. Dec 2016;5(1):25.
205. Deleglise B et al. Synapto-protective drugs evaluation in reconstructed neuronal network. PLoS one.2013;8(8):e71103.
206. Sasaki Y et al. Stimulation of nicotinamide adenine dinucleotide biosynthetic pathways delays axonal degeneration after axotomy. The Journal of neuroscience: the official journal of the Society for Neuroscience. Aug 2006;26(33):8484-8491.
207. Canto C et al. The NAD(+) precursor nicotinamide riboside enhances oxidative metabolism and protects against high-fat diet-induced obesity. Cell Metab.Jun 2012;15(6):838-847.
208. Demarin V et al. Treatment of Alzheimer's disease with stabilized oral nicotinamide adenine dinucleotide: a randomized, double-blind study. Drugs under experimental and clinical research.2004;30(1):27-33.
209. Rex A et al. Treatment with reduced nicotinamide adenine dinucleotide (NADH) improves water maze performance in old Wistar rats. Behavioural brain research. Sep 23 2004;154(1):149-153.
210. Gong B et al. Nicotinamide riboside restores cognition through an upregulation of proliferator-activated receptor-gamma coactivator 1alpha regulated beta-secretase 1 degradation and mitochondrial gene expression in Alzheimer's mouse models. Neurobiol Aging. Jun 2013;34(6):1581-1588.
参考来源:
美国阿尔茨海默病协会
http://www.alz.org
美国梅奥诊所
www.mayoclinic.org
美国神经病学学会
http://www.aan.com
加拿大阿尔茨海默病协会
http://www.alzheimer.ca
加拿大卫生部
http://www.hc-sc.gc.ca
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

